
任安波
(山西大學科學技術史研究所,太原,中國)
1960年代初,在歐洲、加拿大和澳大利亞,萬餘名嬰兒出生時四肢嚴重短小或缺損,如同海豹的鰭狀肢。導致這場新生兒先天性疾病災難的,是一種叫做“反應停”(沙利度胺)的孕婦止吐藥。沙利度胺分子有兩種手性構型:R-構型具有鎮靜效果,S-構型具有致畸性。當時上市的藥物為兩種構型的混合物,既可以讓孕婦止吐又可以導致胎兒畸形。人們由此事件被動認識到分子手性差異對人類的利弊,在後續藥物研發中分離手性分子。
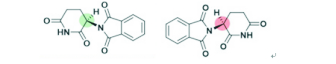
沙利度胺的R-構型(鎮靜)與S-構型(致畸)手性鏡像結構
人類迄今已知的生命體基於L-氨基酸和D-糖。人們設想,是否可以設計並合成基於D-氨基酸和L-糖的生命體,即與已知生命分子手性相反的分子構成的生命形式,與既有生命分子互成鏡像的生命體。但是,現有生命的免疫系統無法識別、環境中的酶也無法降解鏡像生命。鑒於反應停教訓,科學家們開始討論鏡像生命的風險,呼籲暫停合成可覆制的鏡像生命體,以預防其潛在的風險。
從反應停到鏡像生命,人類對應用手性分子的風險認識,從災難發生後的被動補救,轉向風險顯現前的主動設限,構成了一部獨特的手性分子應用社會史。
從構造到構象:分子手性的結構基礎
19世紀初,化學家們意識到元素的原子數量對化合物性質的影響。此後,化學家們又認識到組成相同但原子的連接順序和化學鍵的類型不同,會形成不同構造(constitution)的分子(同分異構體),而且構造相同但原子的空間排布不同,會形成不同構型(configuration)的分子(構型異構體)。後來,人們進一步發現,構型相同的分子僅由於碳-碳單鍵的旋轉,其中的原子或基團就會在空間中產生無數種瞬時、動態的排列形狀,這叫做構象(conformation)。
1848年,巴斯德(Louis Pasteur,1822—1895)利用從葡萄酒發酵副產物中提取的酒石酸銨鈉進行結晶實驗,觀察到可以將其分離成兩種晶體,兩種晶體的水溶液能使偏振光向相反方向旋轉,由此猜想這種差異源於分子在空間結構上的鏡像關系,如同左手與右手一樣對稱卻不能重合,發現了分子的手性。1951年,比傑沃特(Johannes Martin Bijvoet,1892—1980)利用X射線反常散射技術,首次確定了酒石酸的絕對構型,從而確認天然氨基酸為L-型、天然糖為D-型。
然而,即使構型完全相同,分子中的單鍵旋轉,還會使原子或基團產生無數種瞬時的空間排列,這便是分子構象。20世紀初,薩赫斯(Hermann Sachse,1862—1893)突破當時對環碳原子平面結構的認識,提出環己烷非平面折疊構象假說。1943年巴頓(Derek H. Barton,1905—1998) 與哈塞爾(Odd Hassel,1897—1981)利用X射線衍射與構象分析,區分了椅式構象與船式構象兩種基本形態,確證環己烷的椅式構象為最穩定構象。在此基礎上,晶體學家們揭示了蛋白質主鏈的規則構象,即α-螺旋與β-折疊等二級結構。20世紀末朊病毒的發現,揭示出構象在疾病機制中的作用,同一種蛋白質的正常構象與錯誤構象決定健康與疾病。
從構造、構型到構象的認知史顯示,對分子結構的認識與社會應用之間存在著明顯的時滯。1848年發現手性,1874提出四面體模型,1951年確定酒石酸鹽絕對構型,1943年實現構象分析技術,認知都停留在理論上和實驗室里,分子結構差異導致不同應用效果的研究完全被忽視,最終釀成無意的人為悲劇。
從反應停到手性治理:亡羊補牢模式的確立與演進
反應停悲劇的發生,開啟了人們對手性分子的應用研究和治理實踐。兩種構型的沙利度胺的混用不僅導致萬餘名嬰兒的畸形,還使數十萬使用這種混合物的孕婦為避免產出畸形兒而流產,成為有史以來最大的人為醫療災難。這一事件提醒科學家們關注手性分子應用的功能差異,也引發了全球藥物監管的根本變革。
事件之後,不少國家監管機構開始系統性地建立手性藥物的審評制度。1992年,國際人用藥品技術要求協調理事會(ICH)成立,推動全球監管標準的統一。1999年,ICH Q6A指南將對映體雜質控制納入全球藥品質量標準。由此,藥物上市前審評,包括對手性對映體的全面評估,成為一種制度。
與監管制度演進相伴隨的,是不對稱催化制備手性分子的選擇性產物。
反應停事件之後,制藥業采用的辦法是,先制備兩種構型的沙利度胺混合物,再將它們分離開來,保留所需的那種,舍棄不需要的手性對映體。這種辦法既效率低且浪費成本。
1968年,諾爾斯(William S. Knowles,1917—2012)將手性膦配體與銠金屬配合,實現烯烴的不對稱催化氫化,獲得高對映選擇性產物,後將此方法用於生產治療帕金森癥藥物左旋多巴的工業生產。1990年代早期,雷茨(Manfred T. Reetz,1943—2026)和阿諾德(Frances H. Arnold,1956— )開創了定向進化方法,快速優化酶的立體選擇性,拓展了酶在手性藥物合成中的應用。2000年,李斯特(Benjamin List,1968— )和麥克米蘭(David W. C. MacMillan,1968— )等人各自發現了一種有機催化反應,論證了有機催化在不對稱有機催化中的作用。
不對稱催化借助手性配體與金屬離子的配合物、生物酶、不含金屬且結構較簡單的手性有機小分子三種催化劑,使人們能夠在化學合成中精準選擇生成兩種互為鏡像構型的手性分子中的一種,提升了特定手性對映體的生產效率,預防了與之手性相反的對映體分子的風險。
到21世紀初,人類應對手性分子風險的社會史經歷了制度和技術上的變革:確立了以上市前審評為核心的藥物監管框架,實現了不對稱催化選擇性合成特定異構體的技術。
生命設計與鏡像生命:未雨綢繆模式的浮現
反應停事件導致手性分子應用治理走上了上市前審評規制的建立和不對稱催化技術的誕生,但未觸及對尚未出現的基於分子手性的新物質可能給人類帶來的風險防範議題。鏡像生命的設計和研究,回應了這一議題,手性分子治理由之進入未雨綢繆模式時代。
在掌握不對稱催化之後,科學家開始思考能否超越分子手性的選擇,構建與地球生命相反的手性分子系統,即基於D-氨基酸和L-糖的生命體。
蛋白質是由氨基酸聚合而成的生物大分子,是生命功能的主要執行者。氨基酸之間通過脫水形成肽,氨基酸達50個以上者可以形成多肽鏈,多肽鏈折疊形成蛋白質。
早在1993年,肯特(Stephen Kent,1945— )團隊就合成了第一個有功能的鏡像酶D-HIV-1蛋白酶,證明鏡像蛋白質可以正確折疊並具有催化活性。2016年,朱聽團隊合成了鏡像DNA聚合酶(174個氨基酸),實現了鏡像DNA的覆制與轉錄。2022年,該團隊合成了鏡像T7 RNA聚合酶(883個氨基酸),並成功轉錄了鏡像核糖體RNA。鏡像生命的技術可行性開始從理論推演邁向實驗室現實。有人預測,合成完整的鏡像微生物可能只需10至30年。這一趨勢,使科學家們對鏡像生命是否存在性風險的預警,具有了真實的緊迫性。
鏡像生命的風險,在於其自我覆制能力被釋放,可能無法被控制或逆轉。其核心機制是免疫逃逸。地球生命的免疫系統高度依賴於手性識別:T細胞和B細胞通過識別抗原分子上的特定手性結構來啟動免疫反應。鏡像微生物由於手性完全相反,其鏡像蛋白無法被常規酶降解為短肽,因此無法被MHC分子遞呈,適應性免疫系統根本無法辨識。而且,鏡像細菌不會激活補體系統,抗菌肽對手性高度敏感而無法與其有效作用。此外,噬菌體無法識別鏡像細菌表面受體,原生動物無法消化鏡像結構。鏡像微生物一旦逃逸到環境中,可能迅速增殖,對現有生態系統造成不可逆的破壞,可能導致大流行病且幾乎完全不受免疫反應的控制。
為了預防鏡像生命可能引發的災難,2024年12月,來自全球9個國家的38位科學家在《科學》(Science)發文呼籲全球暫停合成可覆制的鏡像生物體。文章附有一份長達299頁的技術報告,詳細評估了鏡像生命的技術前景與潛在風險。作者包括合成生物學、免疫學、生態學等領域的國際領軍人物,其中有兩位諾貝爾獎得主。他們認為,不應創造鏡像細菌或其他鏡像生物,除非出現令人信服的證據表明鏡像生命不會帶來極大危險。這是人類歷史上第一次,在一種風險還處於理論可能階段時,就啟動了全球性、跨學科、前瞻性治理的嘗試。
然而,如何界定足夠的風險證據,僅憑理論推演就限制科學研究,可能構成對學術自由的過度約束。對此,科學界正在形成一種區分策略:鏡像分子的研究(如鏡像藥物、鏡像酶)因具有明確的治療價值且不涉及覆制能力,應繼續推進;而創造可覆制的鏡像生命體,因其潛在的災難性後果,應被劃為紅線。這份倡議也強調,手性分子諸多有價值的應用不帶來類似風險。
目前,這一討論正在全球多個平台上推進。美國、法國、英國、新加坡等國學術機構相繼舉辦了研討會,科學家們呼籲資助方明確表態不支持鏡像生命研究,並建立國際監管框架。
從反應停到鏡像生命,人類走過了從亡羊補牢到未雨綢繆的治理轉型之路。真正的未雨綢繆,不是修好所有屋頂,而是認識到永遠無法修好所有屋頂,並因此保持對未知的敬畏與警覺。分辨分子的左右手,更要學會分辨和預見科技應用效果的兩面性,這或許是這段社會史最深刻的啟示。
原載:加拿大《華僑時報》2026年5月15日第18版“新視界”文化•思想•學術”專版










